来凯在AACR年会发布Afuresertib联合治疗耐药三阴性乳腺癌I期研究积极结果
•中国医学科学院肿瘤医院徐兵河院士牵头,I期入组22例晚期实体瘤患者
•5例三阴性乳腺癌患者治疗时间超过32周,最长1例达73周
•AKT抑制剂的联合方案对乳腺癌表现出初步抗肿瘤活性,值得进一步研究

2024年4月9日——在今天召开的2024年美国癌症研究协会(American Association for Cancer Research, AACR)年会上,来凯医药(股份代码:2105.HK)公布了临床试验项目:AKT抑制剂Afuresertib(LAE002)联合LAE005(PD-L1单抗)+白蛋白紫杉醇用于治疗三阴性乳腺癌的I期研究结果。
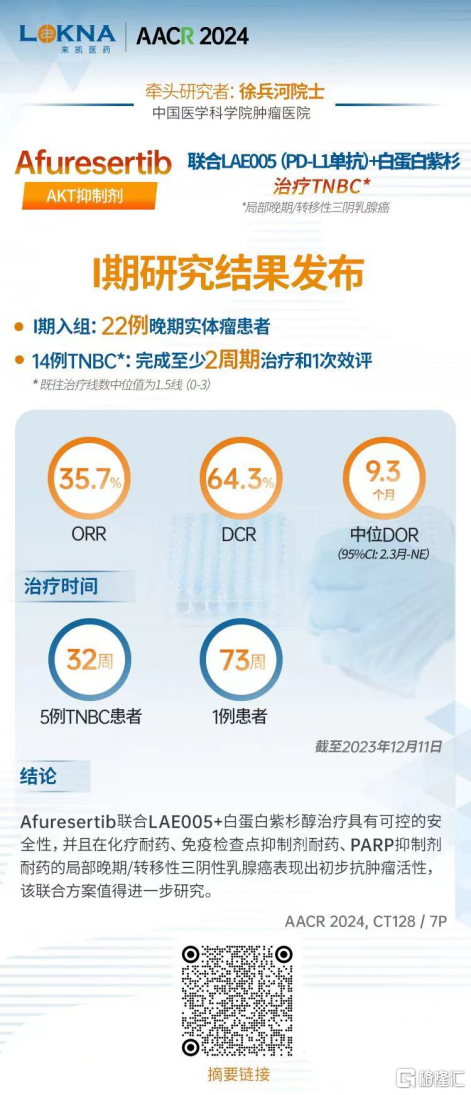
这项由中国医学科学院肿瘤医院徐兵河院士牵头的研究显示,Afuresertib联合LAE005+白蛋白紫杉醇治疗具有可控的安全性,并且在化疗耐药、免疫检查点抑制剂耐药、PARP抑制剂耐药的局部晚期/转移性三阴性乳腺癌表现出初步抗肿瘤活性,该联合方案值得进一步研究。
聚焦三阴性乳腺癌患者
本试验为一项多中心、开放标签、剂量递增的I/II期研究(NCT05390710),于2020年12月获得国家药品监督管理局药物临床试验批准。
I期部分评估Afuresertib联合LAE005+白蛋白紫杉醇治疗晚期实体瘤(主要为三阴性乳腺癌患者)的安全性和耐受性,以及初步抗肿瘤活性。I期部分主要入组标准包括:0-3线标准治疗后进展的局部晚期/转移性实体瘤(三阴性乳腺癌优先),ECOG评分0-1分,具有根据RECIST1.1标准评估的可测量病灶。
截至2023年12月11日,I期入组22例晚期实体瘤患者,其中有14例三阴性乳腺癌患者完成至少2周期治疗和1次评效,其既往治疗线数中位值为1.5线(0-3)。
5例TNBC患者治疗时间超32周,最长73周
中国医学科学院肿瘤医院张频教授透露,本次研究结果显示:在完成至少2周期治疗和1次评效的14例三阴性乳腺癌患者中,最佳疗效评估有5例确认PR(ORR 35.7%),4例SD(28.6%),DCR为64.3%,中位DOR为9.26个月(95%CI: 2.3月-NE)。5例三阴性乳腺癌患者治疗时间超过32周,最长1例达73周。
其中一例多线化疗治疗失败的晚期三阴性乳腺癌患者,无进展生存期(PFS)长达73周。该病例论文入选了《中国临床案例成果数据库》(该论文中截至2023年9月28日该病例PFS为16个月)。
AKT抑制剂在耐药性乳腺癌治疗领域显示潜力
根据2020年世界卫生组织国际癌症研究机构(IARC)发布的数据,乳腺癌是全球女性发病率最高的恶性肿瘤1,其中三阴性乳腺癌约占乳腺癌10-15%,三阴性乳腺癌是指乳腺癌组织免疫组化检查雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体-2(HER2)均为阴性的乳腺癌,是一种侵袭性强、预后差的亚型2。
徐兵河院士表示:"乳腺癌治疗领域在过去十年中取得了长足的发展,但与乳腺癌其他亚型比较,耐药三阴性乳腺癌目前的治疗选择相对有限,是迫切需要解决的临床未满足需求。在本研究中,我们观察到接受治疗的转移性三阴性乳腺癌患者ORR达到35.7%, 以及治疗持续时间5例三阴性乳腺癌患者治疗时间超过32周,最长的1例达73周,该联合方案值得进一步研究。"
来凯医药首席医学官岳勇博士表示,AKT通路活性的上调与许多癌症对标准治疗产生耐药性有关,AKT抑制剂通过降低肿瘤细胞的AKT活性,使既往耐药的治疗重新敏感。"凭借我们对AKT通路激活的充分了解及专业知识,来凯医药已启动五项联合疗法临床项目,覆盖乳腺癌、前列腺癌、卵巢癌及PD-1耐药实体瘤等,其中afuresertib联合氟维司群治疗HR+/HER2-乳腺癌的III期关键试验已经启动。我们相信afuresertib有潜力成为耐药性乳腺癌的有效疗法并惠及大量患者。"
两款自主研发候选药物临床前数据同时公布
在本次AACR年会上,来凯医药总共入选了3份壁报。除了上述临床研究外,还有两项均为自主研发候选新药的临床前数据:一种新型选择性PARP1抑制剂 (LAE119),和一种新型选择性USP1抑制剂(LAE120)。
来凯医药首席科学官顾祥巨博士介绍:此次展示的项目针对两个肿瘤合成致死靶点,在动物模型上都显示出了优异的抗肿瘤活性及安全性。其中LAE119选择性靶向PARP1,相比一代pan-PARP 抑制剂及已知的二代PARP1选择性抑制剂,有更强的DNA捕获能力,对PARP1 表达低的肿瘤细胞有更好的抑制活性。LAE120是一款结构新颖的USP1抑制剂,可诱导USP1不同的构象变化,现已进入临床前预研究(IND-enabling)阶段。
注释:
1.Hyuna Sung, Jacques Ferlay, Rebecca L. Siegel, et al. Global Cancer Statistics 2020_ GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries
2.KWANG-AI WON,CHARLES SPRUCK Triple-negative breast cancer therapy Current and future perspectives (Review)
交易商排行
更多- 监管中EXNESS10-15年 | 英国监管 | 塞浦路斯监管 | 南非监管93.02
- 监管中FXTM 富拓10-15年 |塞浦路斯监管 | 英国监管 | 毛里求斯监管88.21
- 监管中FXBTG10-15年 | 澳大利亚监管 |83.48
- 监管中GoldenGroup高地集团澳大利亚| 5-10年85.87
- 监管中IC Markets10-15年 | 澳大利亚监管 | 塞浦路斯监管91.71
- 监管中CPT Markets Limited5-10年 | 英国监管 | 伯利兹监管91.56
- 监管中AUS Global5-10年 | 塞浦路斯监管 | 澳大利亚监管86.47
- 监管中OneRoyal10-15年 | 澳大利亚监管 | 塞浦路斯监管 | 瓦努阿图监管85.75
- 监管中易信easyMarkets15-20年 |澳大利亚监管 | 塞浦路斯监管85.38
- 监管中FXCC10-15年 | 塞浦路斯监管 | 直通牌照(STP)85.26


